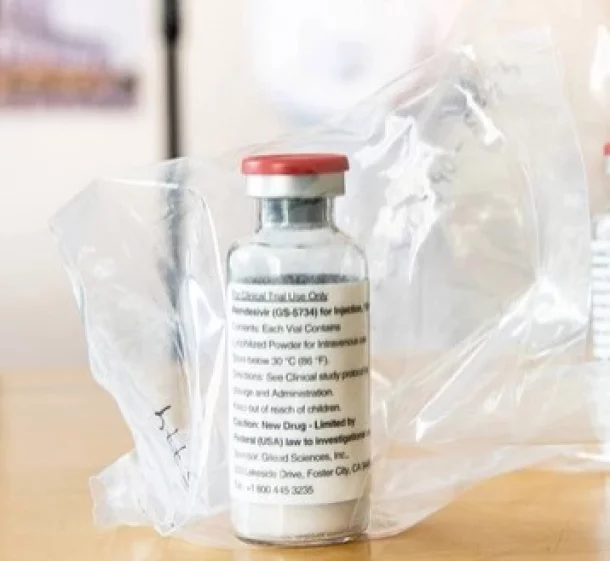
Covid-19: Brasil fica fora da lista que libera patente do remdesivir
POR EGLE LEONARDI
O laboratório americano Gilead abriu mão da patente do antiviral remdesivir, que apresentou resultados moderadamente positivos no tratamento contra a Covid-19. O objetivo é facilitar seu acesso em 127 países. A má notícia é que o Brasil ficou fora dessa lista, sem explicação específica da empresa.
Em comunicado divulgado na terça-feira (12), a empresa disse que assinou acordos de licenciamento voluntário com cinco companhias farmacêuticas especializadas na produção de genéricos, todas com sede na Índia ou no Paquistão.
“Pelo acordo de licenciamento, as empresas têm direito de receber transferência de tecnologia do processo de manufatura do remdesivir para que a produção possa escalar mais rapidamente”, afirmou a Gilead no comunicado.
O efeito esperado da decisão de abrir mão da patente é acesso mais fácil e barato ao medicamento nos locais contemplados.
As empresas que assinaram o acordo com o laboratório são Cipla, Ferozsons, Hetero, Jubilant e Mylan. Elas poderão fixar o preço do produto genérico para venda nos países em que atuarem, a maioria nações pobres de América Latina, Ásia e África.
A lista também inclui alguns países de renda média, potências regionais e Estados emergentes, como África do Sul, Egito, Nigéria, Índia, Indonésia, Paquistão, Tailândia e Ucrânia.
Países ricos ficaram de fora. Na América do Sul, apenas Guiana e Suriname foram incluídos.
O laboratório afirmou à Folha de S.Paulo que a decisão sobre os países contemplados pelo licenciamento voluntário foi baseada na lista do Banco Mundial que define países de baixa e média renda, “com a inclusão de algumas exceções”.
O acordo vale enquanto a Organização Mundial da Saúde mantiver a classificação da crise do coronavírus como pandemia, ou até que surja uma vacina ou remédio mais eficaz para a doença.
Concebido inicialmente para casos de ebola, o remdesivir apresentou alguns resultados positivos no tratamento à Covid-19, reduzindo os prazos de internação de doentes em média em quatro dias.
Outra matéria que pode interessar: Vacina em comprimido para Covid-19: ações de farmacêutica crescem 500%
Em 1º de maio, a FDA, agência norte-americana que regula medicamentos, autorizou o uso emergencial da droga para tentar amenizar os efeitos da pandemia no país, líder de casos e mortes pelo vírus.
No Brasil, o uso do remdesivir ainda não é permitido. Segundo a Anvisa (Agência Nacional de Vigilância Sanitária), houve uma primeira reunião com a Gilead em 6 de maio para discutir a comercialização do antiviral no mercado brasileiro.
“A Gilead tem vários ensaios clínicos em andamento para o remdesivir, com dados iniciais esperados nas próximas semanas. Caso o benefício do medicamento se comprove, a Anvisa possui mecanismos para garantir o acesso célere do medicamento à população”, afirmou a agência em nota.
O laboratório informou que “o plano global de submissão para remdesivir, incluindo o Brasil, está em fase de discussão interna”. Não há prazo para uma definição.
Para o coordenador do Grupo de Trabalho sobre Propriedade Intelectual, Pedro Vilardi, a Gilead levou em conta apenas interesses mercadológicos, ou seja, o lucro que poderá ter vendendo diretamente o produto no Brasil.
Segundo ele, poderia ter sido considerado o fato de que o Brasil, mesmo sendo um país de renda média, tornou-se um dos epicentros mundiais da pandemia nas últimas semanas.
“A boa vontade do laboratório não funciona para garantir acesso equitativo para as populações. O que a gente esperava é que, no maior desafio de saúde do século, o laboratório tivesse um comportamento diferente”, afirmou ele.
Segundo Vilardi, o fato de a empresa ter decidido manter a exclusividade na comercialização do medicamento no Brasil, quando autorizado pela Anvisa, significa risco grande de escassez do produto.
“A Gilead dificilmente será capaz de produzir sozinha o remdesivir para o Brasil, porque Europa e EUA ainda estão enfrentando a doença e demandarão o medicamento em grande quantidade”, afirma.
Embora os resultados apresentados pela droga sejam modestos, qualquer redução de tempo de tratamento numa situação de sistemas de saúde à beira do colapso faz diferença, diz ele.
Com apoio do Grupo de Trabalho sobre Propriedade Intelectual, coletivo de organizações da sociedade civil, um projeto de lei foi apresentado na Câmara por 11 deputados federais de 8 partidos diferentes para quebrar patentes de medicamentos e insumos necessários ao combate à pandemia. O projeto ainda não entrou em pauta, no entanto. A Gilead ainda não definiu o preço do remédio. Um tratamento em geral dura entre cinco e dez dias.
Fonte: Folha de S. Paulo
Participe do nosso grupo de WhatsApp para receber notícias relacionadas à indústria farmacêutica. Clique aqui e faça parte do seleto grupo CDPI Notícias.
